loading, please wait for a moment...
NOTE: You must enable JavaScript in your browser to view this page.

Chapter 10
羧酸 和 取代羧酸
Carboxylic Acids and
Substituted Carboxylic Acids
主讲:唐伟方


羧酸:分子中含 -COOH 的化合物。
通式: RCOOH,可以看作是烃分子中的氢原子被 -COOH 取代所得到的衍生物。
取代羧酸是羧酸烃基上的H被其他原子或基团取代后生成的化合物。
羧酸 羧基

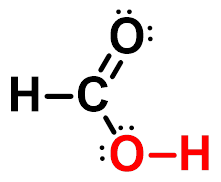
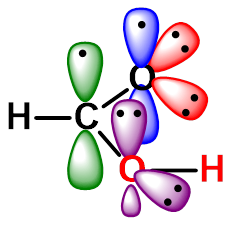
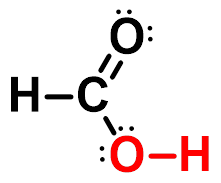
一、结构
酮中C=O双键键长1.20Å;醇中C-O单键键长为1.43Å
甲酸


第一节 结构、分类和命名






|
p-π共轭使键长趋于平均化 |

二、 分类
* 根据含有羧基的数目可分为:
一元羧酸、二元羧酸、多元羧酸
* 根据羧基上所连的烃基 R 不同可分为:
脂肪族羧酸、脂环族羧酸和芳香族羧酸或饱和羧酸、不饱和羧酸,芳香酸苯环上有 羟基的也称为酚酸。
* 根据烃基上取代基的不同可分为:
卤代酸、羟基酸、氨基酸、羰基酸等。
取代酸根据取代基位置不同又可分为:
α -、β -、γ - 等取代羧酸

草酸
(二元酸、脂肪酸)
乙酸
(一元酸、脂肪酸)
丙烯酸
(不饱和酸、一元酸、
脂肪酸)
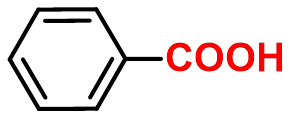
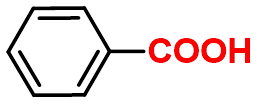
(芳香酸、一元酸)
苯甲酸




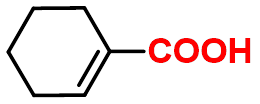
1-环己烯甲酸
(脂环族羧酸、不饱和羧酸)
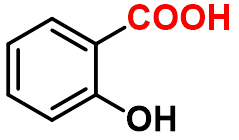
水杨酸
(芳香酸、酚酸)
苯甲酸
(芳香酸)

三、 命名
蚁 酸
formic acid
醋 酸
acetic acid
CH3COOH
HCOOH
肉桂酸
cinnamic acid
草酸
oxalic acid
1、俗名 根据来源:

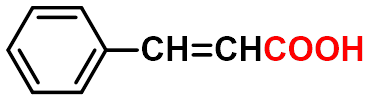

2、系统命名(IUPAC命名)
丙 酸
propionic acid
CH3CH2COOH
|
3-甲基戊酸 α-methylvaleric acid |
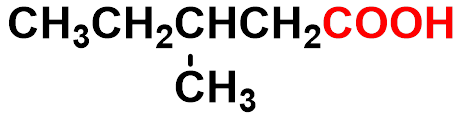
β α
|
β-甲基戊酸 β-methylvaleric acid |

|
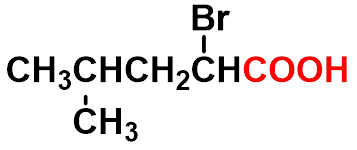
4-甲基-2-溴戊酸 2-bromo-4-methylpenanoic acid |
|
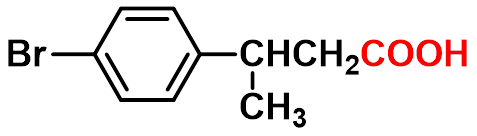
3-(4-溴苯基)丁酸 3-(4-bromophenyl)butanoic acid |

不饱和脂肪酸
选择同时含有羧基和不饱和碳原子在内最长碳链为主链,编号时从羧基碳开始。
|
2-丁烯酸
2-butenoic acid α-丁烯酸 |
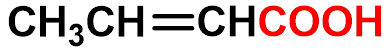

Z-3-甲基-3-戊烯酸
Z-3-methyl-3-pentenoic acid
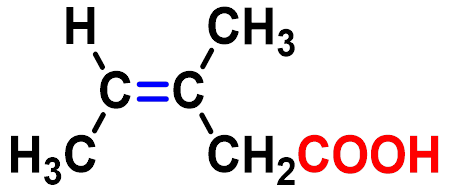

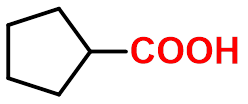
环戊基甲酸
cyclopentanecarboxylic
acid
一元的脂环族羧酸可以将其看做甲酸衍生物,将环做为取代基。
|
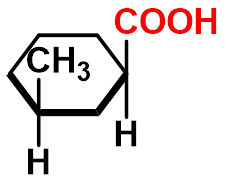
(1R, 3S)-3-甲基环己基甲酸
(1R,3S)-4-methylcyclohexane- carboxylic acid |

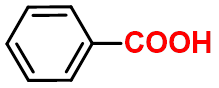
以苯甲酸的衍生物来命名,取代基通过对苯环编号标出,编号从羧基所连碳开始。
苯甲酸
benzoic acid
|
3,4,5-三羟基苯甲酸
(没食子酸) 3,4,5-trihydroxybenzoic acid |
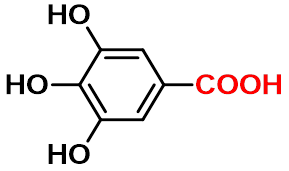

多元羧酸选择含有两个羧基在内的最长碳链为主链,并在“酸”前面表明羧基数目。
己二酸
hexanedioic acid
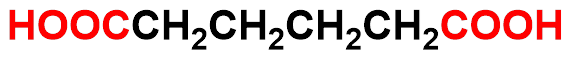

|
(1R,3R)-1,3-环已烷二羧酸
(1R,3R)-1,3-cyclohexane- dicarboxylic acid |
顺丁烯二酸
(马来酸,缩水苹果酸)
cis-butendioic acid
(maleic acid)
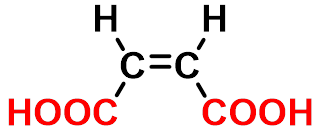
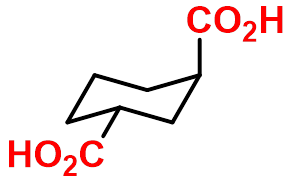

取代羧酸命名将取代的卤素、羟基、氨基等作为取代基,命名与脂肪族羧酸类似,注意: 羰基酸羰基上的氧以“氧代”表示。
|
2-氨基-4-甲硫基丁酸 (蛋氨酸 methionine ) 2-amino-4-(methylthio)butanoic acid |
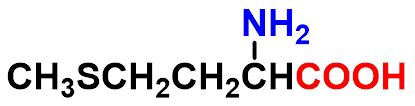

2-甲基-4-氧代丁酸
2-methyl-4-oxobutanoic acid
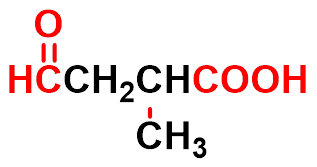

羧酸分子之间的缔合
第二节 物理性质
羧酸的沸点高于相应的醇:羧酸分子间可
形成更多的氢键。羧酸分子主要以二缔合
体的形式存在,沸点较高。
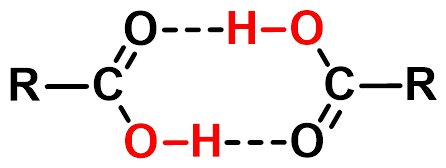

bp: 31oC 80oC 99oC 141oC
能与水形成较多的氢键,水溶性较大,水溶性随其烃基增大而下降。
与水分子之间形成氢键
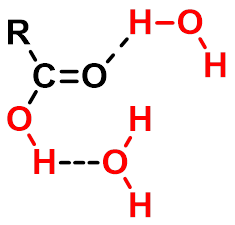
溶解度(g/100ml):
正丁醇 7.98 、丁酸与水混溶

第三节 化学性质
一、 羧酸的酸性


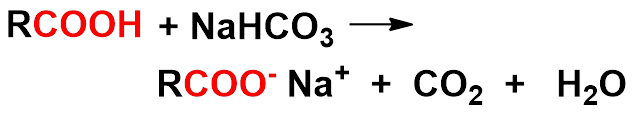
(一) 酸性强弱

羧酸的酸性比酚、醇及其它各类含氢化合物的酸性强
pKa
~ 5
~ 10
~ 16-19

~ 35

醛、酮中羰基的碳氧双键键长(1.20Å)







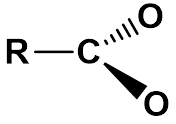

羧酸的酸性强弱还受到碳链上取代基的影响,
取代基的性质、数目、以及取代基在碳链上
的位置等都对羧酸酸性产生影响。
羧酸结构对酸性的影响
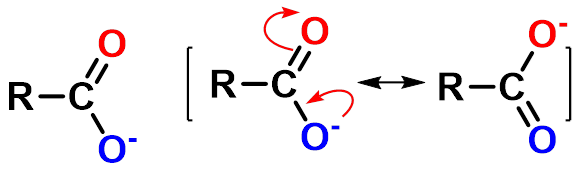
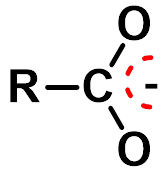
羧酸酸性的强弱取决于电离后所生成的羧酸根负离子的稳定性。总的原则是:
若烃基上的取代基有利于负电荷分散,羧酸根负离子稳定,酸性增强;反之则会使酸性减弱。

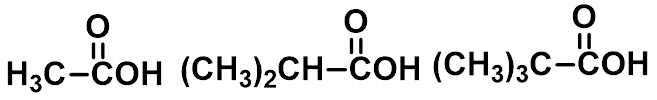
(1) 取代基对脂肪族羧酸酸性的影响
(主要为诱导效应的影响)
①吸电子基使酸性增强,推电子基使酸性减弱;吸电子或推电子能力越强影响越大;基团越多影响越大。
|
HCOOH CH3COOH CH3CH2COOH pKa 3.77 4.74 4.88 |
|
推电子能力: H CH3 CH2CH3 |

|
4.76 4.86 5.05 |
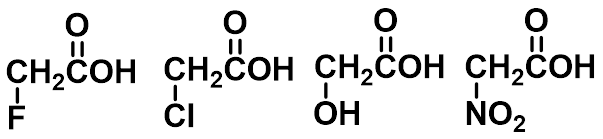
|
2.66 2.86 3.83 1.68 |

|
NO2 > CN > CHO > CO2H > F > Cl > Br > I > C≡CH > OCH3 > OH > C6H5 > CH=CH2 > H |
吸电子诱导效应:
|
推电子诱导效应: |
|
(CH3)3C > (CH3)2CH > CH3CH2 > CH3 > H |
一般在元素周期表中,自左至右或从下
到上吸电子能力依次增强;烃基的C原子在杂化时 S 成分越多,吸电子能力越强。

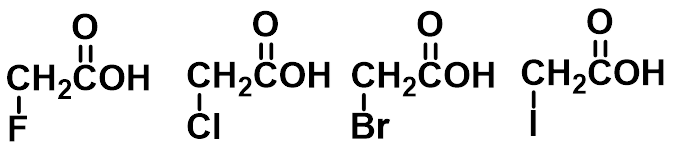
pKa:2.66 2.86 2.90 3.18
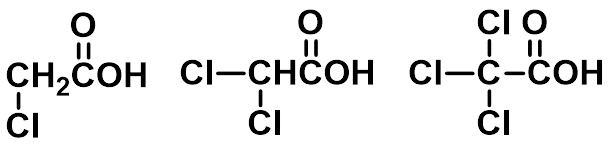
pKa:2.86 1.26 0.64

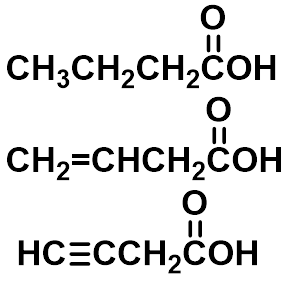
4.82
4.35
3.32
C 原子的吸电子能力: sp>sp2 >sp3
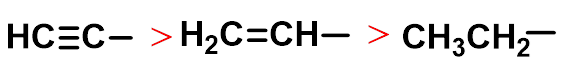

②取代基距离羧基越远,影响越小(诱导效应随距离增加而减弱)
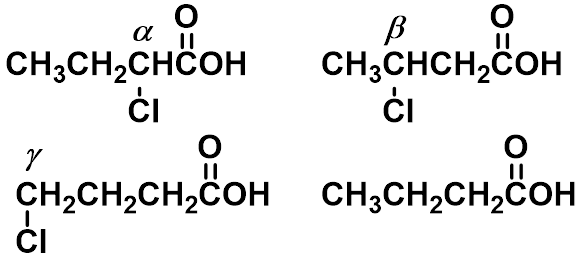
|
2.8 4.1 |
4.5 4.82


③二元羧酸的酸性(K1K2)
pKa1=1.27
pKa=4.74
pKa1=2.85
pKa=3.77
二元羧酸有两个离解常数K1和K2,
酸性由K1决定。

(2)取代基对芳香族羧酸酸性的影响
(1)取代基对脂肪族羧酸酸性的影响
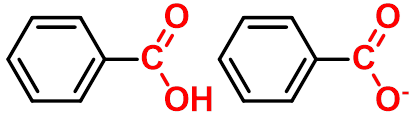
芳香酸苯环上的取代基对其酸性有影响,
随取代基的性质、数目、位置的不同,
影响也不同。

pKa 4.35 4.17 3.40
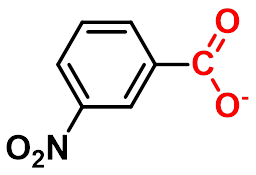
①吸电子取代基使酸性增强,推电子基使酸性减弱。取代基越多,影响越大。
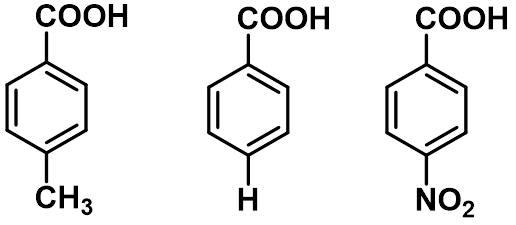

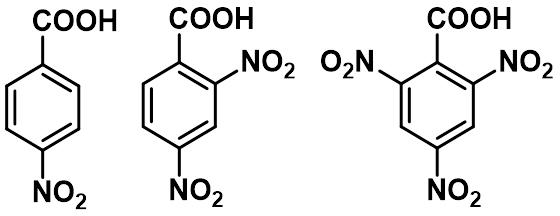
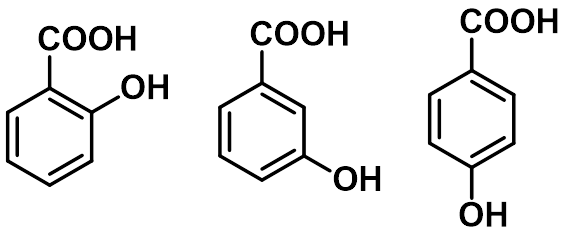
② 对位取代比间位取代的影响大;邻位取代除氨基外,一般都使酸性增强,— 邻位效应。

pKa 2.21 3.46 3.40
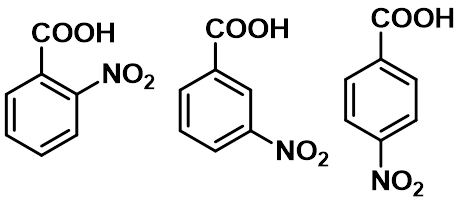
pKa 3.89 4.28 4.35 5.0


诱导效应

共轭效应

诱导效应

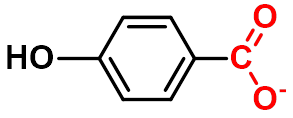
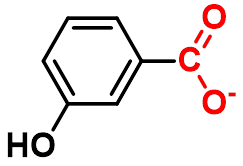
③ -OCH3或-OH在对位时为推电子基,在间位时为吸电子基。
pKa 2.98 4.12 4.54

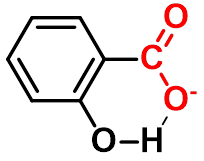



邻位效应:
2.98
4.54
4.08

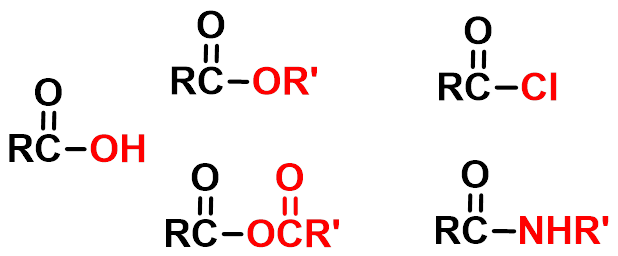
二、羧基中羟基的反应
羧酸
酯
酰氯
酸酐
酰胺

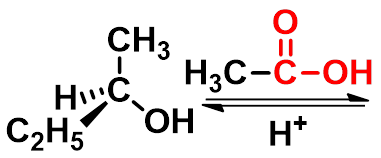
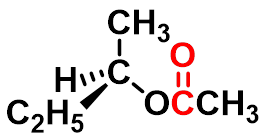
(一)酯化反应-生成酯
可逆反应,常用的催化剂是强酸如:
硫酸,氯化氢或苯磺酸等。
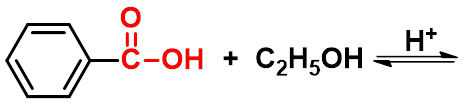
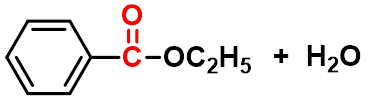

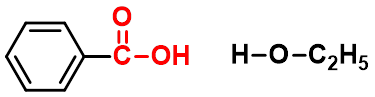
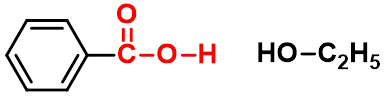
烷氧断裂
酰氧断裂

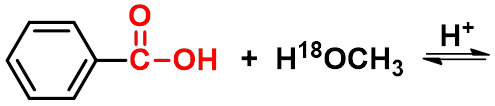
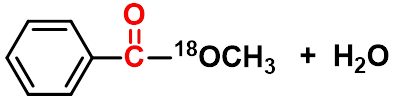


1、 反应机理
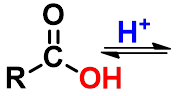
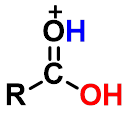


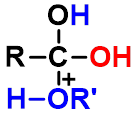
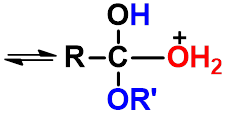

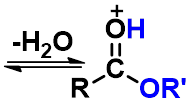
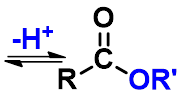
亲核加成
质子转移
消除
脱去质子

先加成后消除,酰氧断裂。
酸的作用:使加成和消除容易。
羧酸与一级、二级醇酯化, 一般是酰氧断裂。三级醇一般是烷氧断裂。



2、 酯化反应活性大小的比较
1、空间位阻:位阻越大,反应越难进行;2、电性效应。(主要考虑空间位阻)。
|
醇:CH3OH > RCH2OH > R2CHOH
酸:CH3COOH > RCH2COOH > R2CHCOOH > R3CCOOH |

|
CH3COOH C2H5COOH (CH3) 2CHCOOH
1 0.84 0.33
(CH3) 3CCOOH (C2H5) 3CCOOH 0.027 0.0016 |

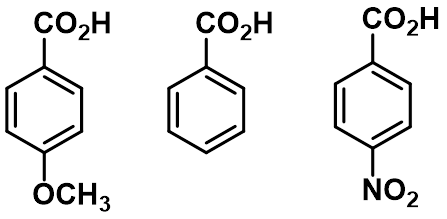

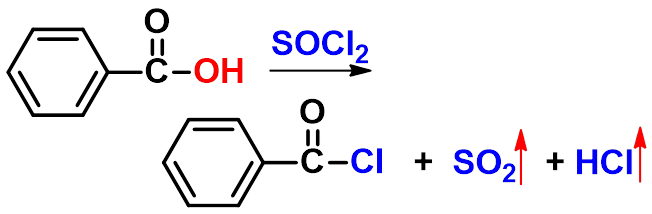
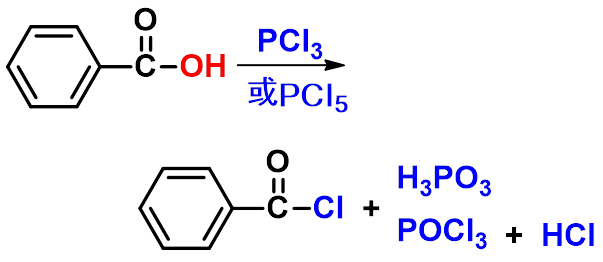
(二)生成酰卤 (acylhalide)(P337)
试剂:亚硫酰氯、三氯化磷或五氯化磷





(三)生成酸酐 (anhydride)
|
脱水剂(如乙酰氯、乙酸酐、P2O5等)存在下加热,分子间失去一分子水生成酸酐(anhydride)。 |
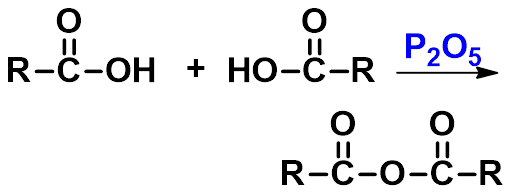

制备混合酸酐
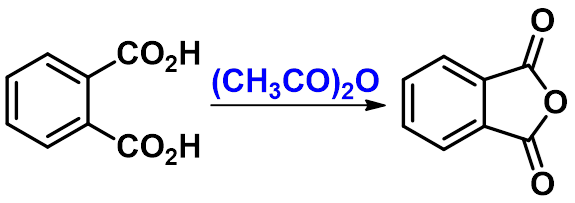
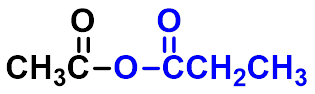


(四)生成酰胺(amide)
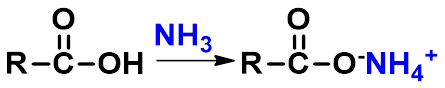
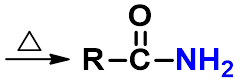
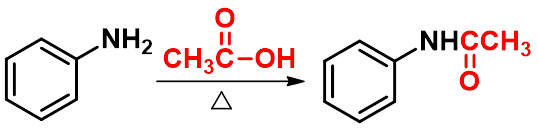

三、还原反应-生成伯醇
|
强还原剂 LiAlH4 将羧酸还原为伯醇 ,分子中的双键不受影响。不能被 NaBH4 还原。 |



四、 α-氢的卤代反应
|
羧酸在少量红磷或三卤化磷存在下与卤素(Cl2或Br2)发生反应,得到α-卤代酸 |

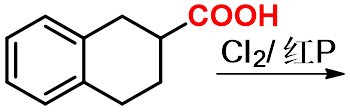
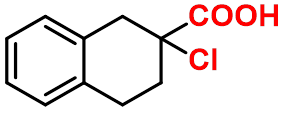

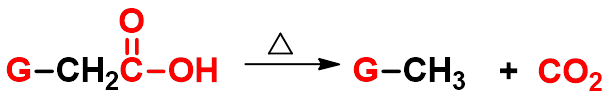
五、 脱羧反应
当 G 为吸电子基团,如:G = COOH, CN, C=O, NO2, CX3, C6H5等时。脱羧反应极易进行。
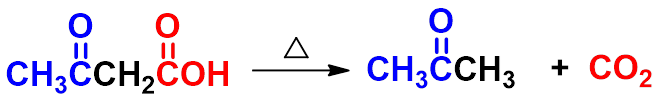

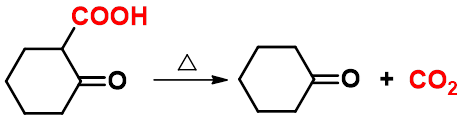
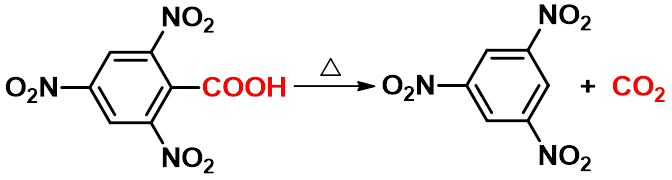

六、 二元酸受热的反应
|
二元羧酸对热较敏感,当单独加热或与脱水剂共热时,随着两个羧基间距离的不同而发生脱羧、脱水或两者兼有的反应。 |
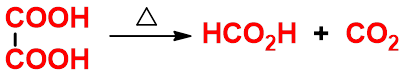
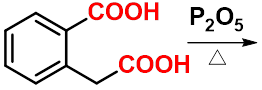
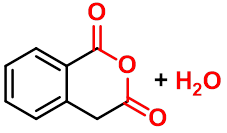
1、 1,2- 或 1,3-二羧酸



|
与脱水剂共热,生成环状酸酐。常用的脱水剂有乙酰氯、乙酸酐、五氧化二磷等。 |
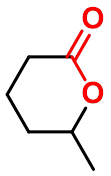
2、 1,4- 或 1,5- 二羧酸

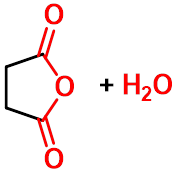

|
两个羧基间隔四个或五个碳原子,受热发生脱水脱羧反应,生成五元或六元环酮。 |
3、 1,6- 或 1,7- 二羧酸



第四节 羧酸的制备
1、氧化法
烯烃、炔烃、芳烃侧链、1级醇、醛酮等的氧化
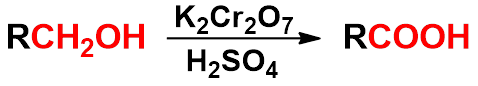
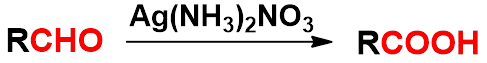

1. 氧化法
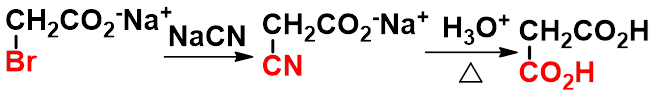
2. 腈水解法
通常只适用于伯卤代烷,仲、叔卤代烷
在氰化钠(钾)中易发生消除反应
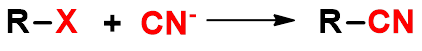

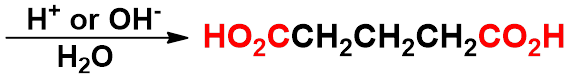

1. 氧化法
2. 腈水解法
|
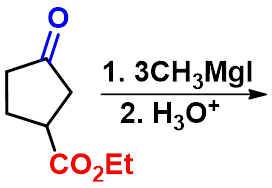
3. 格氏试剂法 |
|
可由伯、仲、叔或芳香卤代烃来制备增加一个碳原子的羧酸。 |

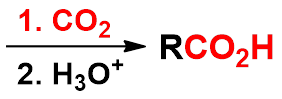
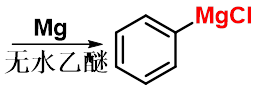
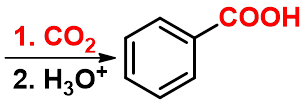

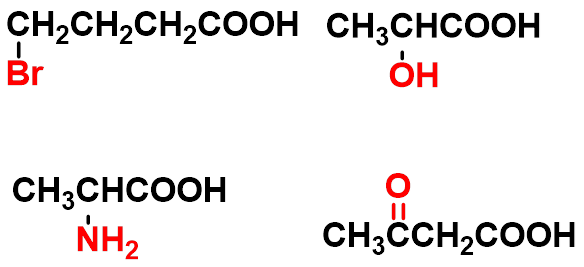
第五节 取代羧酸
卤代酸
羟基酸
羰基酸
氨基酸

1、卤代酸受热的反应(碱性条件)
一、 卤代酸
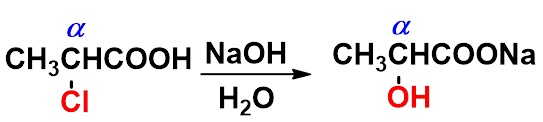

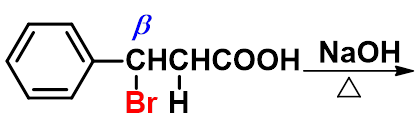
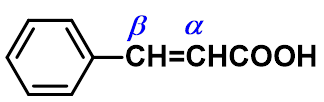


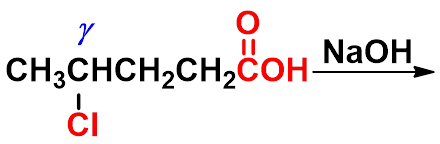

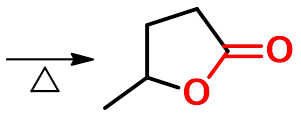
-内酯



|
1、羟基酸的受热反应(酸性条件) |
二、 羟基酸
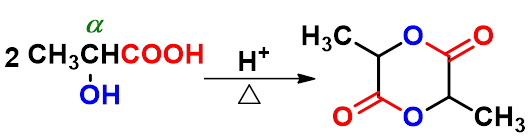
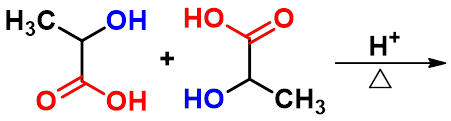
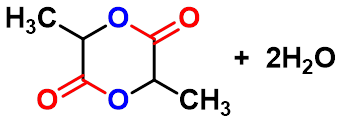
分子间酯化
形成 交酯

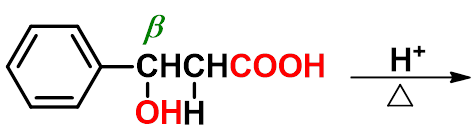
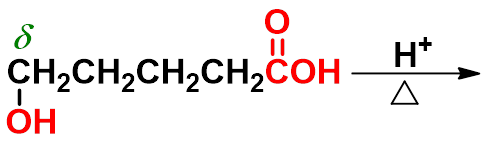
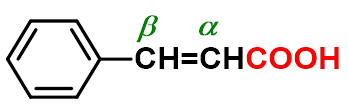
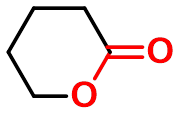

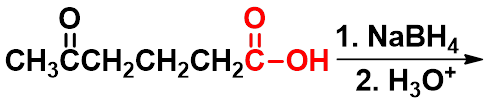
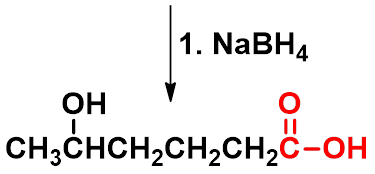
六元环内酯非常容易形成
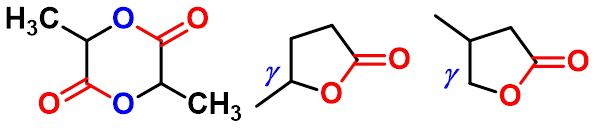
丙交酯
-戊内酯
-甲基- -丁内酯

2、羟基酸的制备
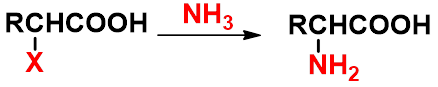
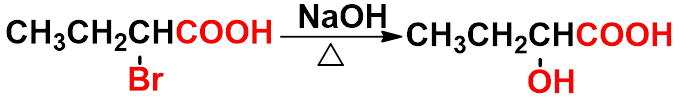
① 卤代酸的水解
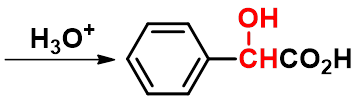
② 氰醇的水解


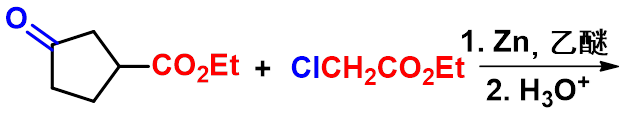
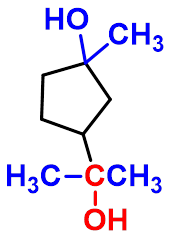
③雷福尔马茨基(Reformatsky)反应
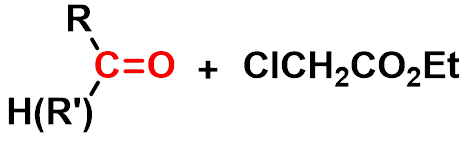
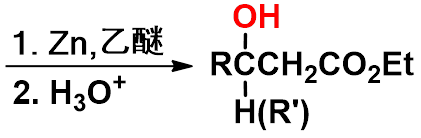
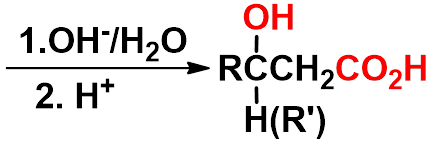

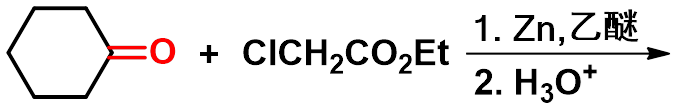
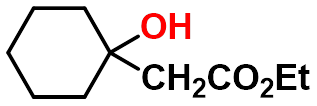
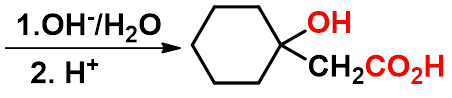



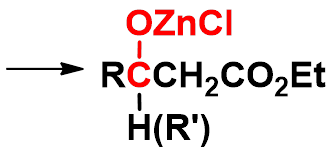
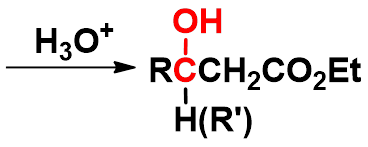
-

有机锌化合物(BrZnCH2COOR)活性比格氏试剂低,不与羧基或酯羰基加成,同时生成的羟基酸不脱羧生成烯。
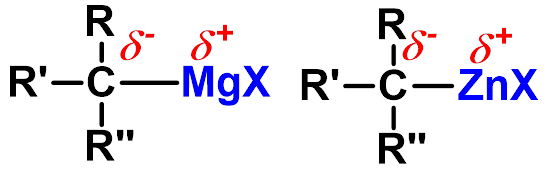

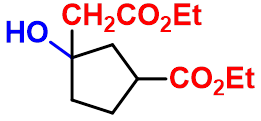

3. 酚酸
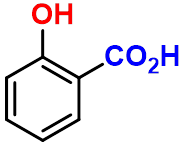
2-羟基苯甲酸(俗称水杨酸)
(2-hydroxy benzoic acid)
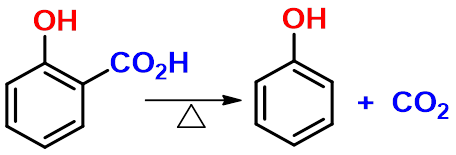

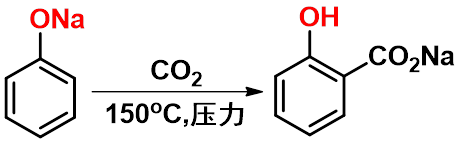
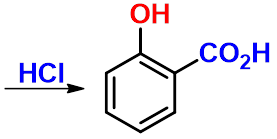
|
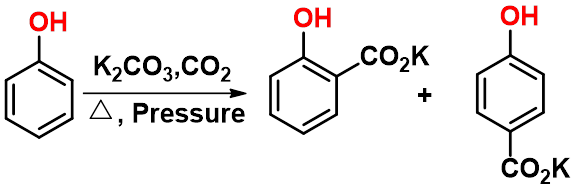
柯尔伯-许密特(Kolbe-Schmitt)反应 |
p323


蛋白质是生命活动的表现形式,氨基酸是构成蛋白质的基本单位,肽或多肽也是由氨基酸组成,其与蛋白质的区别是根据分子量的相对区别。人体内的酶,激素,受体等都是蛋白质。
氨基酸、多肽和蛋白质 p505

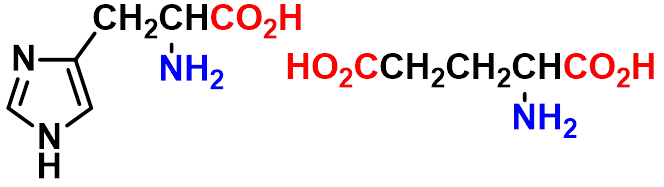
羧酸分子中烃基上的一个或几个氢原子被氨基取代生成的化合物。

组氨酸 谷氨酸(其钠盐即味精)



D型-氨基酸 L型 -氨基酸 D-甘油醛

1、 结构
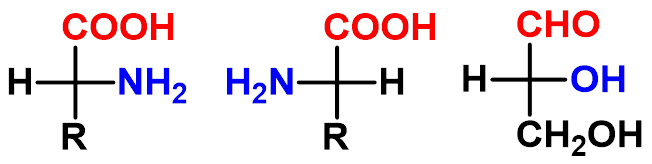

*

氨基酸的命名常根据其来源,用俗名表示,每个氨基酸都有俗名,也用其英文名称的前三个字母来表示:

|
甘氨酸 glycine(Gly) |
|
天冬氨酸 aspartic acid(Asp) |

2、分类和酸碱性

按氨基与羧基的相对位置分:
α-氨基酸,β-氨基酸,γ-氨基酸 等
蛋白质水解后产生的氨基酸,除脯氨酸外,均为α-氨基酸
按氨基酸分子中氨基与羧基的数目来分:
中性氨基酸、酸性氨基酸,碱性氨基酸


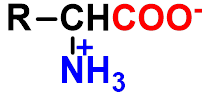
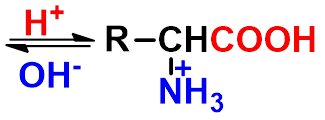
氨基酸分子中既存在酸性基团(-CO2H)
又存在碱性基团(-NH2),以内盐形式
存在。

甘氨酸 天冬氨酸



内盐也称偶极离子(Zwitterion)p511
特点:不溶于有机溶剂,相对能溶于水,当完全以偶极离子形式存在时,其水溶性最小;熔点都很高,类似于盐。
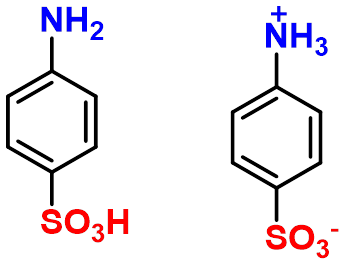


3、氨基酸的等电点

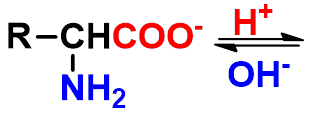
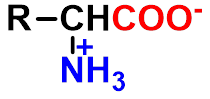


中性氨基酸的水溶液显酸性。

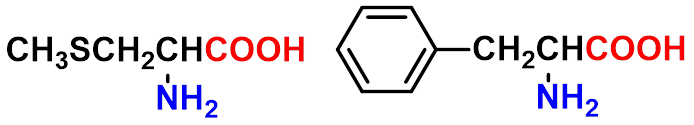
苯丙氨酸

蛋氨酸

酸性指 -N+H3 给出质子的能力,碱性指 -COO-得到质子的能力。以那种离子存在取决于的环境的 pH 值。

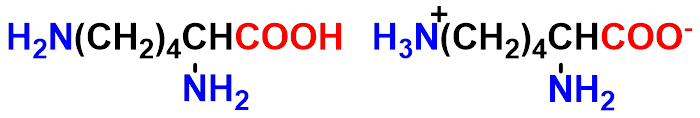
碱性氨基酸分子中碱性基团的数目大于羧基的数目其水溶液显碱性。
赖氨酸
精氨酸
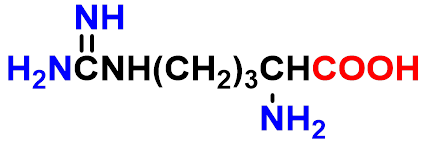

酸性氨基酸分子中碱性基团的数目小于羧基数目其水溶于显酸性。
天冬氨酸
谷氨酸
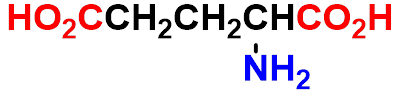
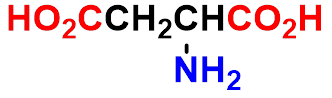


氨基酸溶于水中是否完全以偶极离子的形式存在。与本身结构和溶液的pH值有关 。

中性氨基酸的等电点:pH=6.2~6.8
酸性氨基酸的等电点:pH=2.8~3.2
碱性氨基酸的等电点:pH=7.6~10.8
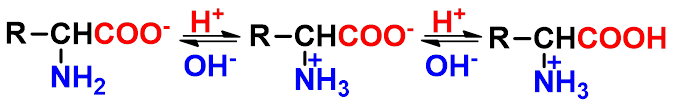

不同的氨基酸有不同的等电点,可用来鉴别氨基酸。
等电点时,以两性离子形式存在的氨基酸浓度最大(在水溶液中),氨基酸的溶解度最小。

可以通过调节溶液 pH 值使氨基酸正好以
偶极离子的形式存在。此 pH 值称等电点。


4、氨基酸的反应
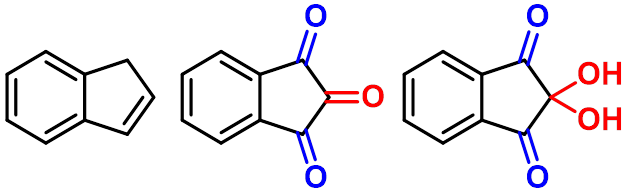
(1)与水合茚三酮的反应
茚 茚三酮 水合茚三酮

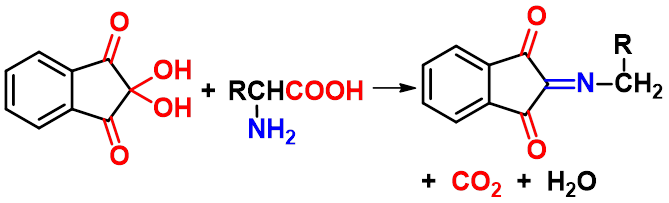
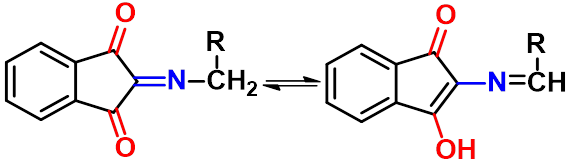

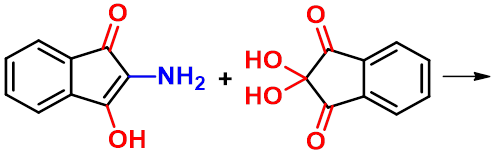
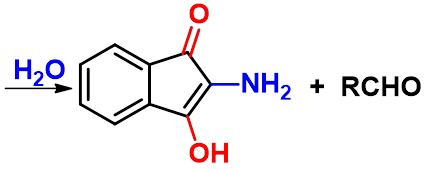
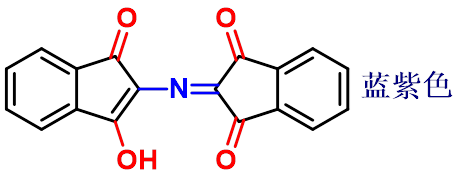

(2)氨基酸受热的反应
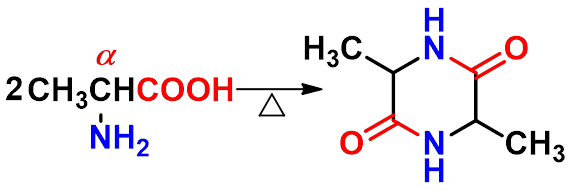
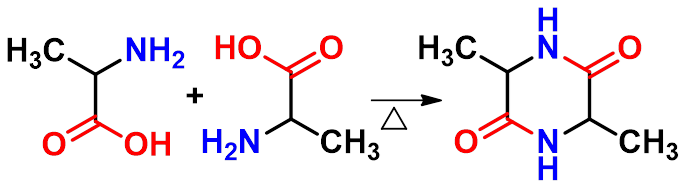

交酰胺


β-氨基酸

γ或-氨基酸 内酰胺
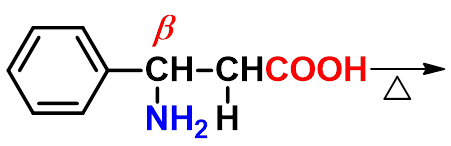
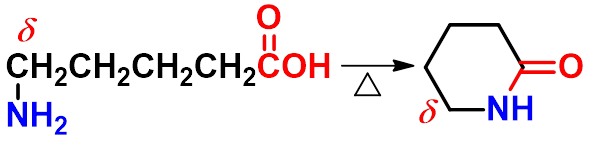
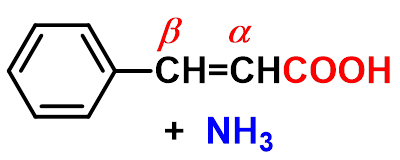
α,β-不饱和酸


二、 多肽和蛋白质
(polypeptides and proteins)

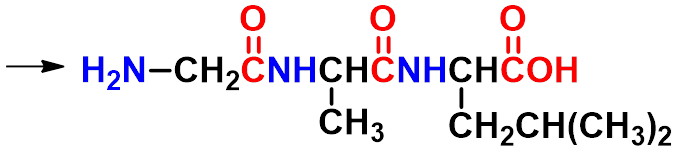
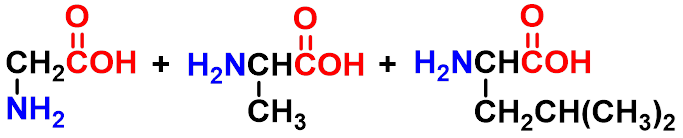
一个氨基酸的羧基与另一分子氨基酸的氨基通过失水反应,形成一个酰氨键,新生成的化合物称为肽,肽分子中的酰氨键叫肽键。二分子氨基酸失水形成的肽叫二肽,多个分子氨基酸失水形成的肽叫多肽。

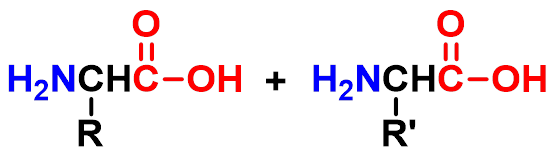
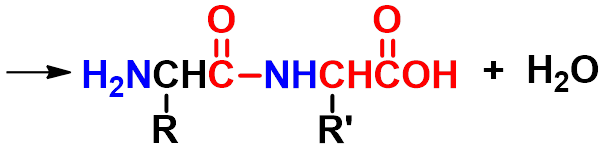
肽键
二肽

|
甘氨酸(Gly) 丙氨酸(Ala) 亮氨酸(Leu) |
|
甘氨酰丙氨酰亮氨酸 (甘-丙-亮)(Gly-Ala-Leu) |



多肽可以经过人工合成,1953年英国科学家桑格
(F.Sanger)测定牛胰岛素一级序列获得了诺
贝尔奖 。1958年 由北京大学和上海生化研究所等
单位联合开始进行牛胰岛素的合成。直到1965年9
月17日成功合成这种由21个氨基酸的A链和30个氨
基酸的B链组成的牛胰岛素,经过严格鉴定,这种
人工合成的结晶牛胰岛素在结构、生物活力、物理
化学性质、结晶形状上都与天然的牛胰岛素完全一
样。人工合成结晶牛胰岛素是世界上第一个人工合
成的蛋白质,为人类认识生命、揭开生命奥秘迈进
了一大步。
|
loading, please wait for a moment... NOTE: You must enable JavaScript in your browser to view this page.
LogsX
|